����
����Ǥ������ |
��ࡡ�ݿ� |
�ڶ���
(��Ǥ�ڶ���) |
�������� |
�ֻ�
(��Ǥ�ֻ�) |
���桡���� |
��ر��� |
���桡���Τ� |
| ����½��� |
���硡�¿�
����������
��¼������
����ͧ��
��С���ǵ
�������龽
���ġ�����
��Ļ��������
|
| ˬ�並��� |
��������
���ġ�ͣ
��������Ϻ
���������
ƣ�桡ɴ���
��߷������
�翹��ͥ
��������
ʿ����������
���ġ���͵ |
| ��������� |
���͡���� |
|
|
 |
 |
 |

�������渦��ֺ¤ϡ�2020ǯ4��˳��ߤ��줿����Ϣ�ȹֺ¤ΤҤȤĤȤ������֤��졢��ǯ��4ǯ�ܤ�ޤ��ޤ��������åդ������ر���������������ʬ�ϡ���Ω���楻��������2009ǯ�����֤��줿����������������ʬ���2009ǯ��2020ǯ�ˤǶ��˸����ԤäƤ��ޤ��������Ԥ�����μ��θ���Τ���θ���ʻٻ���������ˡ�Υȥ�졼����ʥ�ꥵ�����ˤ�2020ǯ������ֺ¤ˤ����Ʒ�³���Ƥ��ޤ��� ���������渦��ֺ¤Ǥϡ���Ȥ������˸���˾��������ơ����ԤΤߤʤ餺�ˤߤ˶줷�വ�Ԥ�����������ˤ���о㳲�����ˡˤ�ʡ���Ȥʤ롢��¸�����ޤ��б��Ǥ��ʤ��ˤߤ��Ф��뿷���ޤ��ޤ�������ȤȤȤ�˶�Ʊ��ȯ���Ƥ��ޤ���
|
|
 |
|
�ٻ���������ˡ�˻붵���Ԥ��뵡����������Ϥ����Ƥ���������ФȻפ��ޤ��� |
 |
|
���ߡ�������ò��������ر���ظ���ʡ���ŷƲ�����ر���ظ���ʡ���������ر���طϸ���ʤ����ر���������˻��ä������˴�Ϣ�θ���˻�ơ��ޤǸ����ʤ�Ƥ��ޤ��� |
 |
|
�������渦��ֺ¤ϡ�����Ϣ�ȹֺ����2020ǯ4�����Ω����4ǯ�ܤȤʤ�ޤ����ֺ¤�̾���̤ꡢ�����Ť���ӻٻ���������ˡ������ȯ���Ƥ���������Ȥȥ��å����Ȥߡ���¸�����Ǥ��б��Ǥ��ʤ������åȥ�ǥ�����ˡ������б����뿷����ȯ���ä������ˤĤʤ��뤵�ޤ��ޤʥ��ơ����ǿʤ�Ƥ��ޤ����ä��ƴ������κ��ѥᥫ�˥���β����ʤɡ���¸����¾�μ����˱��Ѥ���ɥ�å���ݥ�����˥γ�ȯ�⸦����濴�˿����Ƥ��ޤ�����ȤȾ����ͭ��̩�ܤ˶�Ư���뤳�Ȥǡ���û��������ȯ���Ԥ���褦��������Ϣ�Ȥ���פȤ��������ʤ�Ƥ��ޤ���
|
 |
|
 |
 |
 |
 |
|
�����ءʴǸ�ز�2ǯ�� |
 |
|
���ð�ʳح���ǽ�ϼ½��������طϡˡʰ�ز�2ǯ��
�����ð�ؾɸ����ֱ齬���ʰ�ز�3ǯ��
|
 |
|
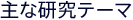 |
 |
 |
| ① | ���Ԥ�ͭ���뤵�ޤ��ޤ��ˤߤ�ȯ�ɤ���Ӥ��λ�³�Υᥫ�˥�������ʤ�Ӥˤ�����ʬ�ҥᥫ�˥������פȤ���������������ȯ���ä��ƥɥ�å�����ݥ�����˥ˤ�����˽����γ�ȯ |
| ② | ������ޤˤ�äƵ����뤵�ޤ��ޤ�������(�ˤߡ����Ӥ졢�ǵ������ǡ���������)�ηڸ��Τ���ο��������ץ������γ�ȯ |
| ③ | �����������Ѥ����ˤ��������ѥᥫ�˥���˴�Ť��������ԥ��������ޤγ�ȯ |
| ④ | ���ռ���ȯ�ɥᥫ�˥����ʬ�ҥ�٥�Ǥβ����ʤ�Ӥˤ��Υᥫ�˥���˴�Ť������ռ���ͽ�ɡ�����ˡ�γ�ȯ |
| ⑤ | ���������Ԥ�QOL�����ʤ�Ӥ˹�����ޤ������ѷڸ��˻�������κ��ѥᥫ�˥���β��Ϥʤ�Ӥ˴��������Ѥ������ι⤤����μ»� |
|
 |
|
 |
 |
 |
 |
- Uezono E, Mizobuchi Y, Miyano K, Ohbuchi K, Murata H, Komatsu A, Manabe S, Nonaka M, Hirokawa T, Yamaguchi K, Iseki M, Uezono Y, Hayashida M, Kawagoe I. Distinct profiles of desensitization of ��-opioid receptors caused by remifentanil or fentanyl: In vitro assay with cells and three-dimensional structural analyses Int J Mol Sci, 24 (9): 8369, 2023.
- Mizobuchi Y, Miyano K, Manabe S, Uezono E, Komatsu A, Kuroda Y, Nonaka M, Matsuoka Y, Sato T, Uezono Y, Morimatsu H. Ketamine improves desensitization of ��-opioid receptor induced by repeated treatment with fentanyl but not morphine. Biomolecules, 12 (3): 426, 2022.
- Komatsu A, Miyano K, Nakayama D, Mizobuchi Y, Uezono E, Ohshima K, Karasawa Y, Kuroda Y, Nonaka M, Yamaguchi K, Iseki M, Uezono Y, Hayashida M. Novel opioid analgesics for the development of transdermal opioid patches that possess morphine-like pharmacological profiles rather than fentanyl: possible opioid switching alternatives among patch formula. Anesth Analg, 134 (5): 1082-1093, 2022.
- Miyano K, Ikehata M, Ohshima K, Yoshida Y, Nose Y, Yoshihara S, Oki K, Shiraishi S, Uzu M, Nonaka M, Higami Y, Narita M, Uezono Y. Intravenous administration of human mesenchymal stem cells derived from adipose tissue and umbilical cord improves neuropathic pain via suppression of neuronal damage and anti-inflammatory actions in rats. PLoS One, 17 (2): e0262892, 2022.
- Miyano K, Hasegawa S, Asai N, Uzu M, Yatsuoka W, Ueno T, Nonaka M, Fujii H, Uezono Y. The Japanese herbal medicine Hangeshashinto induces oral keratinocyte migration by mediating the expression of CXCL12 through the activation of extracellular signal-regulated kinase. Front Pharmacol, 12: 695039, 2022.
- Kuroda Y, Nonaka M, Kamikubo Y, Ogawa H, Murayama T, Kurebayashi N, Sakairi H, Miyano K, Komatsu A, Dodo T, Nakano-Ito K, Yamaguchi K, Sakurai T, Iseki M, Hayashida M, Uezono Y. Inhibition of endothelin A receptor by a novel, selective receptor antagonist enhances morphine-induced analgesia: possible functional interaction of dimerized endothelin A and ��-opioid receptors. Biomed Pharmacother, 141: 111800, 2021.
- Nonaka M, Hosoda H, Uezono Y. Cancer treatment-related cardiovascular disease: current status and future research priorities. Biochem Pharmacol, 190: 114599, 2021.
- Miyano K, Eto M, Hitomi S, Matsumoto T, Hasegawa S, Hirano A, Nagabuchi K, Asai N, Uzu M, Nonaka M, Omiya Y, Kaneko A, Ono K, Fujii H, Higami Y, Kono T, Uezono Y. The Japanese herbal medicine Hangeshashinto enhances oral keratinocyte migration to facilitate healing of chemotherapy-induced oral ulcerative mucositis. Sci Rep, 10 (1): 625, 2020.
- Shindou H, Shiraishi S, Tokuoka SM, Takahashi Y, Harayama T, Abe T, Bando K, Miyano K, Kita Y, Uezono Y, Shimizu T. Relief from neuropathic pain by blocking of platelet-activating factor-pain loop. FASEB J, 31 (7): 2973-2980, 2017.
- Fujitsuka N, Asakawa A, Morinaga A, Amitani MS, Amitani H, Katsuura G, Sawada Y, Sudo Y, Uezono Y, Mochiki E, Sakata I, Sakai T, Hanazaki K, Yada T, Yakabi K, Sakuma E, Ueki T, Niijima A, Nakagawa K, Okubo N, Takeda H, Asaka M, Inui A. Increased ghrelin signaling prolongs survival in mouse models of human aging through activation of sirtuin1. Mol Psychiatry, 21 (11): 1613-1623, 2016.
|
 |
|
 |
 |
 |
 |
|
- AMED ��Ū������ż��Ѳ��������
�֥ҥȤ��ռ���ȿ�Ǥ����ȼ���Ω���ռ���ǥ���Ѥ��Ƥΰ��ռ������ֲ������ʤ�Ӥ����������Ǥ�ͭ�Ѥʡ֤��ռ�PDX��ǥ�פγ�Ω�Ȥ��γ��ѡ�
2022-2024ǯ�� �ʾ�ࡧ��ɽ����ԡ�
- AMED ��Ū������ż��Ѳ�������ȡ֤��Ԥˤ�����Ѹ夻����ͽ�ɤΥץ쥷������ǥ�����γ�ȯ��
2022-2024ǯ�� �ʾ�ࡧʬô����ԡ�
- AMED ��������ʸ������
�֤��ԤΤ�����ȯ�ɤ�ͽ�ɤ����λ�������Ӹ���Ǵ������������˻�Ⱦ���ÿ���Υ�ܥ�������Ϥˤ��쥹�ݥ�����Х����ޡ������γ�ȯ�ʤ�Ӥˡ־ڡפβĻ벽�Ȥ��������ѡ�
2021-2023ǯ�� �ʾ�ࡧ��ɽ����ԡ����ʬô����ԡ�
- AMED ��Ū������ż��Ѳ��������
�֤����ѥϥ��ꥹ�����ԤνѸ夻����ͽ�ɤˤ��������ƥ����ͭ�����Ȱ������˴ؤ���¿���߶�Ʊ����ո����ץ饻���оȥ����ಽ��ӻ��
2021-2023ǯ�� �ʾ�ࡧʬô����ԡ�
- AMED ������������Ĵ�¡�ɾ���������
�֥ҥ�iPS ��˦ͳ�迴�ں�˦���Ѥ���������ޤο�����ɾ��ˡ�γ�ȯ�ȹ��ɸ�ಽ��
2021-2023ǯ�� �ʾ�ࡧʬô����ԡ�
- ʸ���ʳؾʲʳظ������������ ������(C)
�֤�������������PHLDA3�ι������������ǽ�㳲���Ф����������Ѥβ�����
2022-2024ǯ�� �����桧��ɽ����ԡ���ࡧʬô����ԡ�
- ʸ���ʳؾʲʳظ������������ ������(C)
�������Ѥε����ˤ������ԥ����ɼ����Υ����ʥ�Τߤ�������Ǥ��벽��ʪ��������ȯ��
2021-2023ǯ�١ʾ�ࡧ��ɽ����ԡ����ʬô����ԡ�
- ʸ���ʳؾʲʳظ������������ ������(C)
�֥��ԥ����ɼ����Τκ�˦��ɺߤȳ����Ѳ��˴�Ť���Ŭ�ʥ��ԥ����ɽ缡��Ϳˡ�γ�Ω
2021-2023ǯ�١ʾ�ࡢ���ʬô����ԡ�
- ʸ���ʳؾʲʳظ������������ ������(C)
�֤�����лٻ����Ťˤ�����Ⱦ���ÿ����ͭ���������餫�ˤ��뤿��δ��õڤ��������
2021-2023ǯ�١ʾ�ࡢ���ʬô����ԡ�
- ʸ���ʳؾʲʳظ������������ ������(C)
�ֿ����ǥ������륰��������Τ�𤷤�����ʪ��ڥץ��ɤ��Ѥ����������������������
2021-2023ǯ�١ʾ�ࡧʬô����ԡ�
- ʸ���ʳؾʲʳظ������������ ������(C)
�֤��ռ�������ǽ�㳲�����������β����ȱ�ư����ӱ��ܲ����ˤ�뿷������ˡ�γ�ȯ��
2021-2023ǯ�١����桧ʬô����ԡ�
- ʸ���ʳؾʲʳظ������������ ������(C)
���������ˤ��Ф���ҥȴ��շϴ���˦�ˤ�����˺��ѤΥᥫ�˥�������Ȥ��������ѡ�
2020-2023ǯ�١ʵ����ɽ����ԡ���ࡧʬô����ԡ�
|
 |
|
 |
 |
 |
 |
��Ʊ����������
������ҥĥ�顢��������ҡ���컰��������ҡ��ޥ�۳�����ҡ�
��������������ҡ�������ҥХ����ߥ�ƥ���������ѥ��������������QUINERGY
|
 |
|
 |
| |
|